-
E-Mail-Adresse
ec@hkaco.com
-
Telefon
13412598543
-
Adresse
Gebäude T6 der PCI Future Community, 30 Kaitai Avenue, Huangpu, Guangzhou
Guangzhou Hongke Elektronik Technologie Co., Ltd.
Mikrofluide Blut-Hirn-Barriere-Chip Übersicht

Blut-Hirn-Barriere (BBB) ist eine selektive Barriere, die das Gehirn und das zentrale Nervensystem (ZNS) schützt und eine stabile innere Umgebung aufrechterhaltet. Es besteht aus endotelialen, peripheralen, glialen und extrazellulären Zellen, die die Integrität der Barriere gewährleisten. Blut-Hirn-Barrierefunktionsstörungen sind mit Krankheiten wie Alzheimer und Parkinson verbunden und können schädliche Substanzen in das zentrale Nervensystem bringen. Das heutige Blut-Hirn-Barrieremodell ist in der Lage, diese Erkrankungen durch die Entwicklung gezielter Therapien und die Identifizierung potenziell neurotoxischer Fremdstoffe besser zu untersuchen, was einen wichtigen Schritt in der Neurowissenschaft und Pharmakologie darstellt.[1-2].
Traditionelle Forschung der Blut-Hirn-Barriere (BBB-Methoden, wie Transwell Komoroexperimente und Tiermodelle, haben Einschränkungen wie übermäßige Vereinfachung, schlechte physiologische Korrelationen und Rassendifferenzen.
Mikrofluide Blut-Hirn-Barrieremodell (μBBB) löst diese Probleme durch die Simulation der Blut-Gehirn-Barrierefunktion im Körper. Diese Modelle können die Umgebung präzise steuern, Zellkultur unterstützen, Schnittstress ausüben und die Umgebungsbedingungen des menschlichen Gehirns replizieren. Mikrofluidisierte Blut-Gehirn-Barrieregeräte ermöglichen hochauflösende Bildgebung, intrazelluläre Überwachung und extrazelluläre Reaktionsanalyse, was sie zum idealen Werkzeug für die Forschung von Erkrankungen des zentralen Nervensystems, therapeutisches Screening und neurotoxische Tests macht. Sie bieten ein großes Potenzial für den Fortschritt der Blut-Hirn-Barriere-Forschung[2].
Eine ideale in vitro Blut-Hirn-Barriere (BBB-Modelle sollten die Schlüsselmerkmale der Blut-Hirn-Barriere im Körper replizieren, einschließlich:
lEndothelzellen (ECs) Bildung von 3D-Gefäßstrukturen
lInteraktion zwischen Zellen
lSchnittspannung durch Flüssigkeitsströme auf Endothelzellen
leine dünne und poröse Grundfolie (BM)
Simulation der Blut-Hirn-Barriere in vitroBesitzenEiner der Herausforderungen besteht darin, die natürliche Substanzmembran genau zu replizieren, die eine entscheidende Rolle bei Prozessen wie Zelldifferenzierung, in-vivo-Gleichgewicht, Gewebeaufrechterhaltung und strukturelle Unterstützung spielt. Idealerweise sollte eine künstliche Substratmembran aus biokompatiblen Materialien hergestellt werden, die etwa eine Dicke von 100 Nanometer.
1 Konstruktion von Mikrofluidgeräten
1.1 Sandwich-Design
Diese mikrofluidgestützte Blut-Hirn-Barriere-Konstruktion ist gekennzeichnet durch zwei obere und untere Schichten Polydimethylsiloxan (PDMS) Kanäle, in der Mitte durch poröse Membrane getrennt. Normalerweise werden Polycarbonatfolien mit einer Durchmesserbereiche von 0,2 bis 3 Mikrometer verwendet, ähnlich dem Transwell-System. Endotelzellen werden in der Regel im oberen Kanal geimpft, während Peripheren, Asteroiden oder andere Gehirnzellen im unteren Kanal kultiviert werden.
Andere transparente Membrane, wie Tetrafluorethylen, ermöglichen eine hochauflösende Bildgebung sowie die Überwachung des biomolekularen Transports und des Zellwachstums in Echtzeit. Darüber hinaus umgekehrt Zell Impfung Konfiguration, d. h. Kultur von Endothelzellen in einer dreidimensionalen angiogenartigen Struktur des unteren Kanals (ECs), Die gleichzeitige Impfung von Peripheren und Astrozyten im oberen Kanal verbessert die Beobachtung der interzellulären Wechselwirkungen.
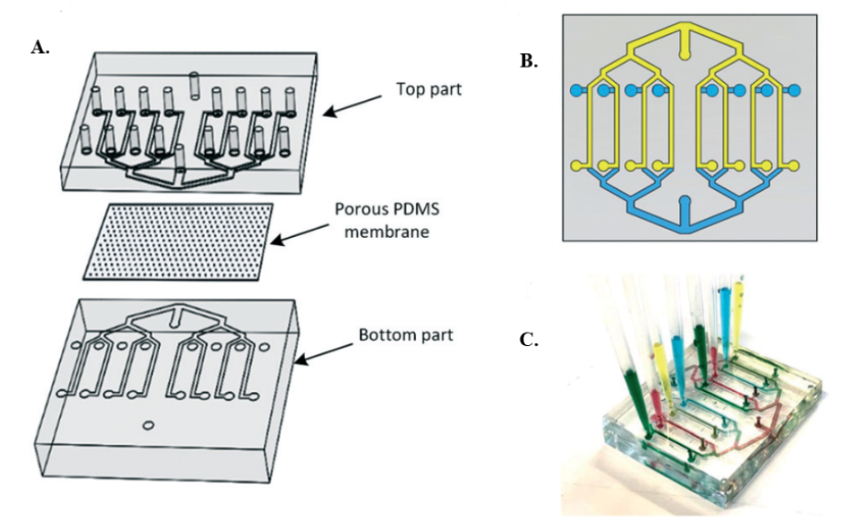
Bild1 Blut-Gehirn-Barriere-Sandwich-Design-Symbol auf dem Chip. (a) Auflösungsdiagramm des Chips, einschließlich der oberen und unteren Teile,
Jeder enthält acht Kanäle, bestehend aus porösen PDMS Membran Trennung. (b) Schemation des Entwurfs der zweistöckigen Ausrüstung,
Eigenschaften sind zwei identisch. PDMS-Komponenten, eine umgekehrt und mit der anderen verklebt. (C) zeigt, dass acht verschiedene Bedingungen in zwei Schichten erzeugt werden[2]
1.2 Parallele Konstruktion
Zwei horizontal angeordnete Kanäle PDMS-Mikrokanal-Array-Trennung ersetzt herkömmliche Polycarbonatmembranen durch PDMS-basierte Mikrosäulen-Membranen (3-Mikrometer-Spalt)[3]Diese Konstruktion ist in der Lage, mit Asterozyten oder Hirntumorzellen zu kultivieren und vereinfacht den Montageprozess, indem keine zusätzlichen chemischen Modifikationen erforderlich sind. Das Planlayout verbessert die Interaktion zwischen den Zellen und die Bildgebung.
Das Gerät ist gekennzeichnet durch eine Gewebekammer mit zwei Blutgefäßkanälen mit Flüssigkeitseingängen auf beiden Seiten, die auf Mikroskopträgerschienen montiert sind und mit einem Kunststoffrohr für den Eingang in den Kanal ausgestattet sind.
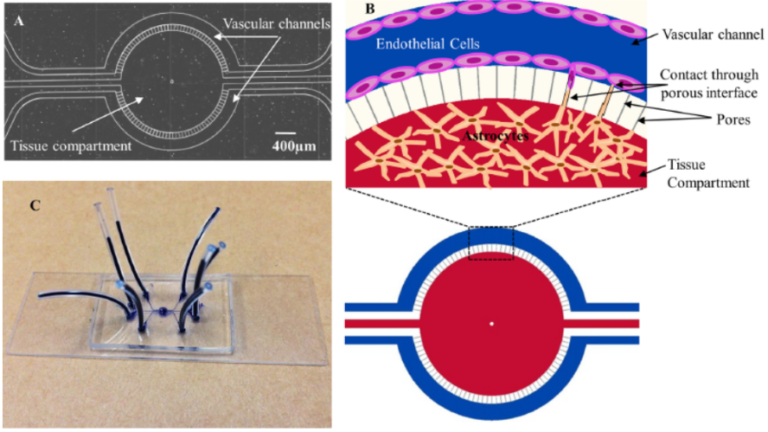
Bild2 Bild der Blut-Hirn-Barriere auf dem Chip.A. Die Abbildung zeigt die Gewebekammer im Zentrum der Anlage,
Es ist umgeben von zwei unabhängigen Gefäßkanälen mit Flüssigkeitseintrittsöffnung.B. Schema der Zellkultur in diesem Design.
C. Das Gerät ist auf einem Mikroskopträger montiert und ist mit einem Kunststoffrohr (dunkelblau) für den Zugang zu verschiedenen Gefäßkanälen und Gewebekammern ausgestattet[3].
1.3 Dreidimensionale Strukturgestaltung
TraditionDas PDMS μBBB-Modell verwendet rechteckige Mikrokanäle, die zu ungleichmäßigen Strömungen und ungleichmäßigen Scherkräften führen und das Verhalten der Endothelzellen beeinflussen. Um dieses Problem zu verbessern, verwenden einige Modelle zylindrische Mikrokanäle für gleichmäßige Schnittkraft, wie z. B. Mikrovaskuläre Rohre auf Basis von 3D-Kollagen (Durchmesser 75-150 μm), die den Rohrdurchmesser durch die Flüssigkeitsströmungsgeschwindigkeit genau steuern und in μBBB-Geräte integrieren.
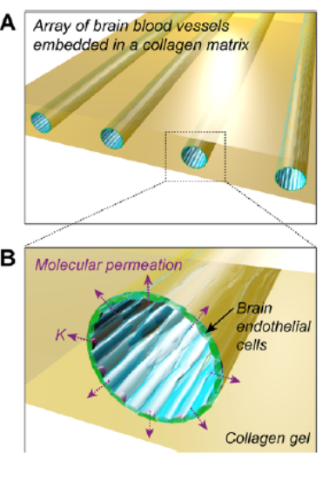
Bild3 Mikrovaskuläres Hirnsystem[4]
2 Blut-Gehirn-Barriere-Chip-Experimentiergerät
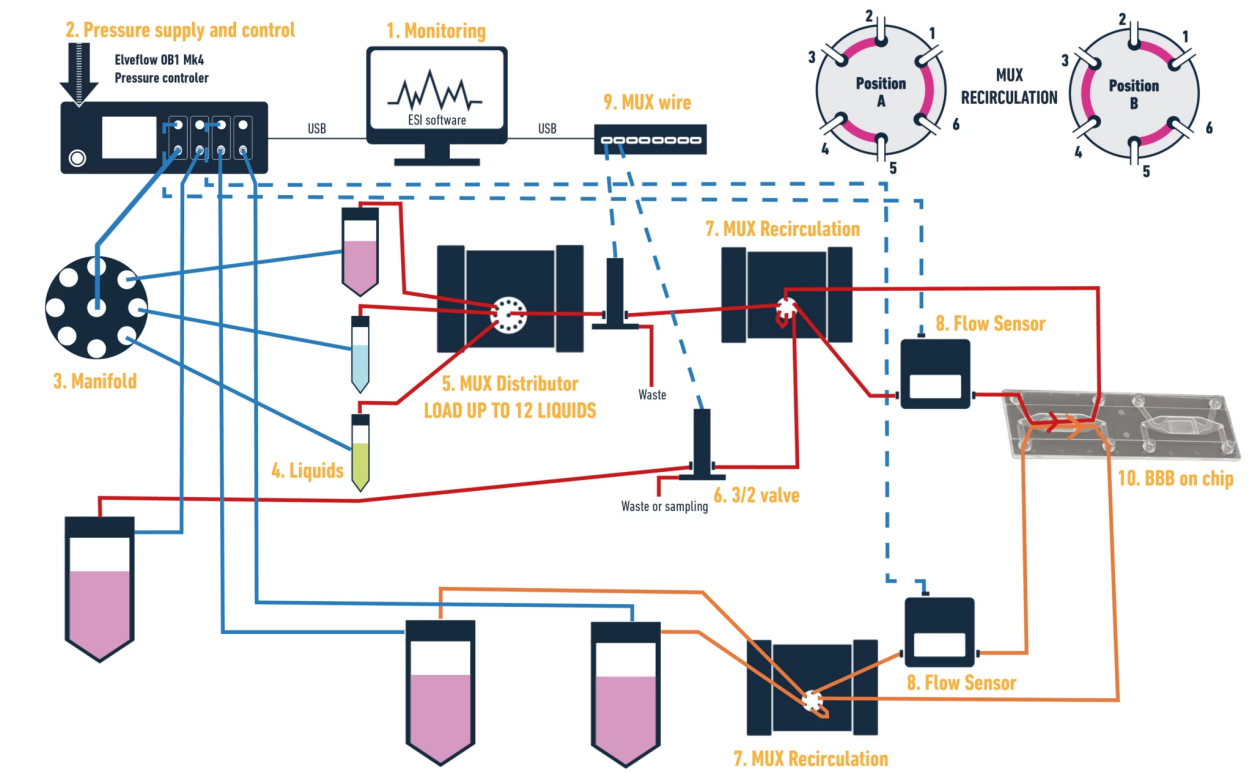
Blut-Gehirn-Barriere-experimentelle Geräte auf dem Chip integriert:
1. OB1 Durchflussregler
2. Diskrimination
3. MUX-Umlaufventil
4. MUX Verteilerventil
5. MUX Leitungen
6. Drei Durchgänge. / Zwei Ventile
7. Mikrofluidgestützter Durchflusssensor
8. Verbindungen, Rohrleitungen und Ruhr-Verbindungen
9. Speicherbehälter
10. Mikro-Fluid-Chip für Blut-Hirn-Barriere-Chip-Modelle
11. Mikrofluidisierungssoftware
2.1 Vorteile von Elveflow-Geräten
1. OB1 Druckregler
lPräzise Fluidstromsteuerung:Der OB1 verfügt über einen piezoelektrischen Regler, der eine schnelle und stabile Druckregelung ermöglicht. Diese Genauigkeit gewährleistet, dass die Mikrofluidumgebung physiologische Bedingungen genau simulieren kann, was von entscheidender Bedeutung ist, um die dynamischen Eigenschaften der Blut-Hirn-Barriere genau zu reproduzieren.
lDynamische InfusionsfähigkeitIn Blut-Hirn-Barriereinrichtungen auf Chips ist die Aufrechterhaltung einer angemessenen Schnittspannung für die Funktion der Endothelzellen von entscheidender Bedeutung.OB1 ermöglicht die Kontrolle des Flüssigkeitsflusses, ermöglicht eine dynamische Infusion und simuliert die Blutflussbedingungen im Körper, wodurch die physiologische Relevanz des Modells verbessert wird.
2. MUX Verteilerventil
lAutomatische InjektionsreihenfolgeMit diesem Ventil können verschiedene Reagenzien, Medikamente oder Medien in den Blut-Gehirn-Barrierechip programmiert transportiert werden. Diese Automatisierung ist von entscheidender Bedeutung für die Durchführung dynamischer Infusionsexperimente, die die in vitro-Bedingungen genau simulieren, was die physiologische Relevanz des Modells erhöht.
3. MUX-Umlaufventil
lSimulation physiologischer Bewegungsbedingungen:Das MUX-Recycling-Gerät ermöglicht eine präzise, programmierbare Recycling von Flüssigkeiten, die entscheidend sind, um die Schnittspannung und die Flüssigkeitsdynamik zu replizieren, die die Endothelzellen in der Blut-Hirn-Barriere erleben.
lKontrollierte Recycling sorgt für realistische BlutflussmusterDies ist entscheidend für die Aufrechterhaltung der Form und Funktion der Endothelzellen.
lDrogentests und ToxizitätsscreeningMedikamente oder Nanopartikel auf kontrollierte Weise einführen und wiederzirkulieren, um ihre Interaktion mit der Blut-Hirn-Barriere im Laufe der Zeit zu untersuchen.
lDynamisches Co-KultivierungssystemEs gewährleistet eine kontinuierliche Infusion, die für die Vitalität der Zellen und die Aufrechterhaltung enger Verbindungen von entscheidender Bedeutung ist.
lVerringerung des Verschmutzungsrisikos: geschlossenen ZyklusgroßDie Verringerung des Verschmutzungsrisikos ist eine häufige Herausforderung bei offenen Intrusionssystemen.
3 Anwendungsbereiche
3.1 Modellierung von neurologischen Erkrankungen
lHirntumorBlut-Hirn-Barriere (Das BBB-Modell wird verwendet, um die Wechselwirkungen von Gliom-Startzellen (Schlüsselfaktoren für Hirntumorenfälle) in ihrer Umgebung zu untersuchen. Darüber hinaus ermöglicht die Verwendung von in vitro Blut-Hirn-Barriere-Systeme ein klareres Verständnis der Mechanismen der Hirntumormetastase. Durch die Integration von Glioblastoma-Sphären von Patienten in Mikrofluidsysteme bieten diese Modelle eine effiziente Plattform für das Screening von Medikamenten mit starker Tumortödlichkeit.
lNeurologische StörungenEntzündliche Reaktionen bei neuropathischen Läsionen werden durch die Ansammlung und Migration von Immunzellen (einschließlich Neutrophilen, Glialen und Astrozyten) verursacht. In neurologischen Erkrankungsmodellen wie der Alzheimer-Krankheit wird die Neurozzündung durch die Aktivierung von Mikroglia und Astrozyten angetrieben. Aktivierte Immunzellen freisetzen entzündliche Zytokinen, einschließlich Tumor-Necrotifaktoren (TNF)-α und Interleukin (IL)-1. Während dieser Reaktion zerstören Zytokinen und Immunzellen die Blut-Hirn-Barriere (BBB), was häufig dazu führt, dass Blut in das Gehirn infiltriert und somit irreversible Gehirngewebsschäden verursacht.
3.2 Neurobiologische Forschung
Steuerung der Mikroumgebung um die Neuronenzellen, einschließlich der interzellulären und zellulären und extrazellulären Matrix, innerhalb einer Mikrofluidplattform (Die Wechselwirkungen zwischen ECM) schaffen eine Mikroumgebung ähnlich dem Körper für die Differenzierung von neuronalen Stammzellen in Bestandteile des Nervensystems.
Durch die Kombination von Mikrofluidtechnik mit Neurobiologie können einige technische Herausforderungen auf diesem Gebiet wie die Kultivierung des zentralen Nervensystems (Neuronen, die Trennung von Axonen, die Modellierung kultivierter Neuronen, die Führung des Neuronenwachstums zur Simulation von Axonschäden und die Untersuchung von Prozessen wie lokaler Proteinsynthese, Axonregeneration und Axontransport innerhalb der Axonen.
3.3 In vitro Medikamentenentwicklung
Das Blut-Hirn-Barriere-System auf dem Chip bietet eine Plattform zur Beurteilung der Penetration von Medikamenten durch die Blut-Hirn-Barriere unter dynamischen und physiologisch relevanten Bedingungen und behebt die Einschränkungen herkömmlicher in vitro-Modelle. Sie sind in der Lage, Träger-Nanopartikel zu bewerten, einschließlich Rezeptor-vermittelter Transformation und Nanoträger-Optimierung für gezielte Lieferung im zentralen Nervensystem. Indem sie die zelluläre Komplexität der Blut-Hirn-Barriere replizieren, helfen diese Modelle, Neuroprotektoren und Antikörper unter krankheitsspezifischen Bedingungen zu testen. Die integrierten Sensoren ermöglichen Einblicke in Drogentoxizität, neuronale Aktivität und synaptisches Verhalten. Mit Zellen von Patienten, die das individuelle Medikamentsscreening und die Forschung auf spezifische Erkrankungen unterstützen[4].
3.4 Gehirnachsforschung auf Chips
Multi-Organ-Chips bieten eine Plattform für die Untersuchung der Interaktionen zwischen dem Gehirn und anderen Organen im Kontext von Krankheiten und Medikamentenentwicklung. Sie sind in der Lage, komplexe Erkrankungen wie Lungenkrebs-Hirnmetasen zu untersuchen, bei denen dynamische Prozesse repliziert und detailliert untersucht werden können. Diese Chips helfen auch, das Mikrobiom aufzudecken. - Darm - Kommunikationswege in der Gehirnachse, die erklären, wie sich die Darmgesundheit auf neurologische Erkrankungen auswirkt. Durch die Simulation miteinander verbundener Organsysteme wie die Leber-Gehirn-Achse bei Hepatoencephalopathie oder die Immunregulation durch die Gehirn-Milz-Achse bietet der Multi-Organ-Chip einen umfassenden Ansatz zum Verständnis von ganzheitlichen Erkrankungen. Ihre Fähigkeit, dynamische physiologische Umgebungen zu simulieren, hat bahnbrechende Forschung in der Kommunikation zwischen Organen und der Entwicklung von Therapien gefördert.
Referenzen
1. X. Chen; C. Liu; L. Muok; C. Zeng und Y. Li, Dynamic 3D On-Chip BBB Modell Design, Entwicklung und Anwendungen in neurologischen Erkrankungen, Zellen, 2021
2. M. Sacharowa; M. A. Palma do Carmo; M. W. van der Helm; H. Le-Der; M. N. S. de Graaf; V. Orlova; A. van den Berg; A. D. van der Meer; K. Broersen und L. I. Segerink, Multiplexe Blut-Hirn-Barriere-Organ-auf-Chip, Lab on a Chip, 2020.
3. S. P. Deosarkar; B. Prabhakarpandian; B. Wang; J. B. Sheffield; B. Krynska und M. F. Kiani, Eine neue dynamische neonatale Blut-Hirn-Barriere auf einem Chip, PlosOne, 2015
4. J.A. Kim; H.N. Kim; S-K. Ich; S. Chung; J.Y. Kang und N.Choi, Kollagen-basiertes Gehirnmikrovaskularmodell in vitro mit dreidimensionaler gedruckter Schablone, Biomicrofluidics, 2015
5. X. Wang; Y. Hou; X. Ai; J. Sun ; B. Xu; X. Meng; Y. Zhang und S. Zhang, Potenzielle Anwendungen der Mikrofluidik basierten Blut-Hirn-Barriere (BBB) - auf Chips für in vitro-Drogenentwicklung, Biomedizin & Pharmakotherapie, 2020